结直肠癌是最常见的恶性肿瘤之一,随着人口老龄化、遗传、生活方式(如喝酒、吸烟、饮食等)以及环境的改变,结直肠癌的高发病率居高不下,目前,我国结直肠癌的发病率位居全部恶性肿瘤的前三,其病死率也高达第4位[1]。据2015年一项流行病学数据显示,尽管肿瘤的根治性切除的改进,增加了患者的5年生存率,我国结直肠癌病死率高达50%以上[1-2]。而结直肠癌是一种具有高度特异性的恶性肿瘤,其在临床病理特征、组织形态、免疫表型、治疗效果以及生物学行为等方面存在较大差异,肿瘤的转移和复发仍然是患者重要的死亡原因[3-4]。
组蛋白修饰在疾病的研究中备受关注,其中组蛋白甲基化修饰及乙酰化修饰在肿瘤方面的研究更为常见。组蛋白乙酰化修饰可影响细胞内染色质的结构,从而参与了相应位点的基因转录及调控,在肿瘤细胞生长和分化过程中起重要作用。因此,本实验着重观察结肠癌细胞株SW480及结肠癌组织中组蛋白乙酰化修饰的相应位点的变化情况,以期了解组蛋白乙酰化修饰在结肠癌中的修饰情况,为后续进一步的有关结肠癌在组蛋白乙酰化修饰方面更深入的研究做好前期实验基础。
1 材料与方法
1.1 实验材料
人正常结肠上皮细胞株NCM460及人结肠癌细胞株SW480均购于上海歌凡生物科技有限公司。使用NCCN指南中关于结肠癌的诊断标准,通过腹部增强CT、肠镜及病理活检选取了10例明确诊断为无远处转移结肠癌的可行手术治疗的患者,取出患者手术切下的肠段,分别选取正常结肠组织及结肠肿瘤组织(均通过病理检测证实)。
1.2 主要试剂
胎牛血清购自Gibco公司;DMEM培养基购自HyClone公司;DNaseⅠ、彩虹Marker购自Solarbio;细胞裂解液、蛋白酶抑制剂、BCA蛋白定量试剂盒、Alexa Fluor488标记山羊抗小鼠IgG(H+L)、DyLight549标记山羊抗兔IgG(H+L)购自上海碧云天生物技术有限公司;E-Plate检测板购于埃森生物(杭州)有限公司,acH3K9、acH3K14、acH3K18、acH3K27抗体均购自Abcam公司。
1.3 实验方法
1.3.1 体外细胞培养 用含10%胎牛血清及含青、链霉素的DMEM培养基置于5%、37 ℃细胞培养箱内培养,定期换液传代,取对数生长期细胞用于实验。
1.3.2 提取细胞核及核蛋白制备 将细胞及组织利用核浆分离技术提取目的核蛋白。按每1×106个细胞加入裂解液100 µL核蛋白酶抑制剂1 µL的比例冰上裂解30 min,1 200 r/min低温离心10 min,提取细胞的核蛋白,-80 ℃保存。
1.3.3 组织标本处理 将选取的正常结肠组织及结肠肿瘤组织,用EP管分装,存于-80 ℃冰箱备用。
1.3.4 Western blot分析组蛋白乙酰化状态 将提取的细胞及组织的核蛋白,以100 g/L或120 g/L的SDS-PAGE分离,湿法电转移法转膜,室温下摇床封闭1 h,加入不同浓度的一抗(组蛋白乙酰化修饰位点 acH3K9、acH3K14、acH3K18、acH3K27抗体1:1 000,H3抗体1:400),4 ℃过夜,TBS洗涤液洗膜后分别放入用TBS按1:1 000稀释的辣根过氧化物酶标记的羊抗兔二抗以及羊抗鼠二抗,室温下摇床作用1 h,TBS洗涤液洗膜后化学发光法显色,X线片曝光,以H3为内参照。
1.4 统计学处理
用SPSS 20.0统计软件进行分析。数据均采用均数±标准差(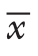 ±s)表示,多组间比较采用单因素方差分析(ANOVA),组间两两比较采用最小显著性差异法(LSD法)。P<0.05为差异有统计学意义。
±s)表示,多组间比较采用单因素方差分析(ANOVA),组间两两比较采用最小显著性差异法(LSD法)。P<0.05为差异有统计学意义。
2 结 果
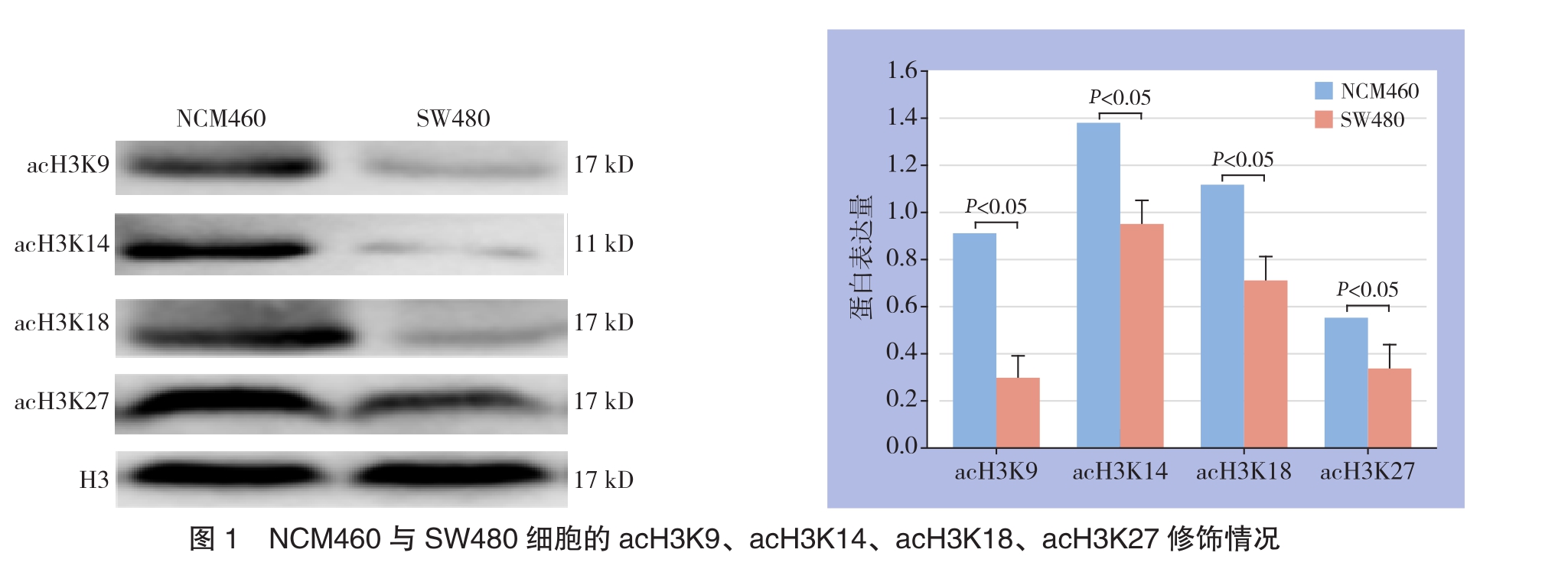
2.1 Western blot法检测正常结肠上皮细胞与结肠癌细胞组蛋白乙酰化修饰水平
使用Western blot检测NCM460与SW480细胞的acH3K9、acH3K14、acH3K18乙酰化修饰水平。结果显示,与NCM460比较,SW480细胞组蛋白acH3K9、acH3K14、acH3K18、acH3K27修饰水平明均显下调(均P<0.05)(图1)。
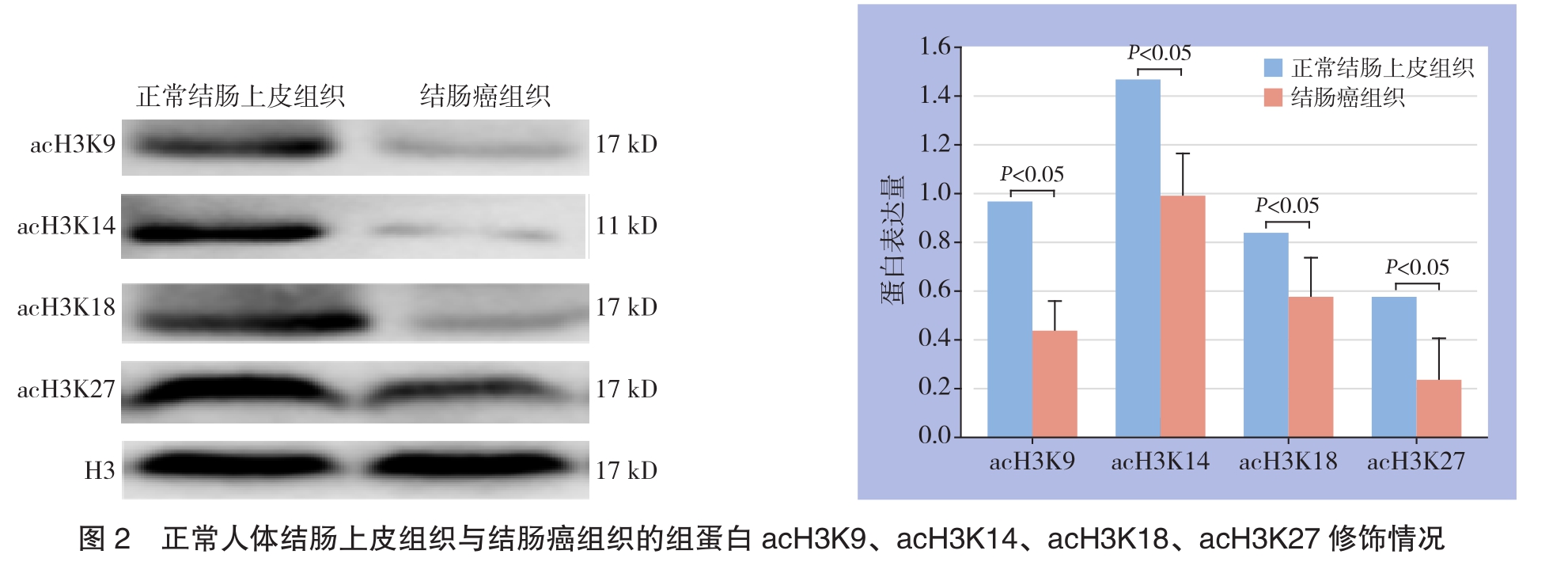
2.2 Western blot法检测肠癌患者手术标本中乙酰化修饰水平
使用Western blot法检测肠癌患者手术切除的肿瘤肠段组织和同一肠癌患者手术切除后非肿瘤肠段组织的组蛋白acH3K9、acH3K14、acH3K18、acH3K27乙酰化水平进行检测,与正常结肠上皮组织相比,结肠癌组织的组蛋白acH3K9、acH3K14、acH3K18、acH3K27修饰水平均明显下调(均P<0.05)(图2)。
3 讨 论
结直肠癌是世界上最常见的恶性肿瘤之一,但其发病机制仍不明确,因肿瘤的早期症状不明显,大部分肿瘤患者确诊时已处于中晚期,尽管以根治性切除为主的治疗方法已经很大程度上延长了患者的生存期,但其晚期转移和复发仍然是结直肠癌患者死亡的重要原因[5]。
近年来,表观遗传学的研究逐渐被认为与肿瘤发生发展的重要的因素之一[6],表观遗传是指不通过改变DNA序列就能影响基因表达的、可以遗传的遗传修饰方式,而组蛋白修饰包括甲基化、乙酰化、磷酸化、泛素化等[7-8],这些修饰的程度与状态决定着基因是否表达[7]。有研究[9]发现,组蛋白乙酰化在疾病的发生发展中起着重要的意义,而其中H3K9乙酰化是修饰基因转录调控的重要机制。组蛋白乙酰化修饰多在H3赖氨酸残基上的9、14、18、23位点和H4精氨酸残基上的5、8、12、16位点,而这些位点可激活基因也可沉默基因[10-11]。组蛋白乙酰化修饰是通过组蛋白乙酰基转移酶(histone acetyltransferases,HATs)和组蛋白去乙酰化酶(histone deacetylases,HDACs)联合调控,取决于HAT和HDAC的动态平衡[12]。组蛋白的尾部有多种化学修饰作用,这些修饰可以影响基因的表达(例如:H3和H4发生乙酰化后有利于激活基因转录,而H3K9发生甲基化后可以抑制基因转录)[13]。组蛋白乙酰化转移酶的主要功能是对核心组蛋白N端25~40个氨基酸范围内的赖氨酸进行乙酰化修饰,HAT将乙酰辅酶A上的乙酰基转移到组蛋白N端赖氨酸的ε-氨基上,从而中和了其正电荷,增加了疏水性,削弱了DNA与组蛋白的相互作用,有利于转录因子与DNA的结合,促进转录[14]。
近年的研究[15]显示,肿瘤的发生不仅与DNA甲基化有关,同样的,组蛋白乙酰化也是参与其中。有研究[16]发现,组蛋白乙酰化缺陷在急性白血病的发病中起着重要的作用,也有相关报道[17]证实正常乳腺组织中乙酰化的组蛋白H3、H4的表达均较乳腺癌高。关于组蛋白乙酰化在肠癌中的修饰表达,国外已有相关的报道[18]显示:组蛋白的异常乙酰化与结直肠癌的发病有关。
本实验的研究结果发现:与NCM460相比,SW480细胞组蛋白acH3K9、acH3K14、acH3K18、acH3K27修饰下调;与正常结肠上皮组织相比,结肠癌组织的组蛋白acH3K9、acH3K14、acH3K18、acH3K27修饰下调。有学者[19]研究证实:在结直肠癌与其他肿瘤中,组蛋白乙酰化降低;然而,对特定部位的检查表明,乙酰化可以上调或下调。而Fraga等[20]使用Western blot分析发现,在结直肠癌细胞系H4K16中出现乙酰化降低,而在未分化结肠腺癌中观察到H4K12和H3K18的低乙酰化,在分化良好的结直肠肿瘤中,其乙酰化修饰程度增加[21]。与这些发现相反,H3K9的低乙酰化状态与肿瘤组织学类型呈正相关,在分化良好的肿瘤中观察到H3K9Ac乙酰化水平降低[22]。在其他实体肿瘤中,即肺腺癌和鳞状细胞癌,H3K27乙酰化的增加在肿瘤部分比在相应的基质中更明显[23]。在前期有关肝癌中组蛋白乙酰化修饰水平也出现了类似的变化[24]。因此,后续的实验研究将更深入的研究组蛋白乙酰化修饰在结肠癌中体内及体外实验其染色质免疫共沉淀等相关实验,以期组蛋白乙酰化修饰在结肠癌中的机制。
[1]Aran V, Victorino AP, Thuler LC, et al.Colorectal Cancer:Epidemiology, Disease Mechaanisms and Interventions to Reduce Onset and Mortality[J].Clin Colorectal Cancer, 2016, 15(3): 195-203.doi: 10.1016/j.clcc.2016.02.008.
[2]Chen W, Zheng R, Baade PD, et al.Cancer statistics in china,2015[J].CA Cancer J Clin, 2016, 66(2):115-132.doi: 10.3322/caac.21338.
[3]Tang W, Zhu Y, Gao J,et al.MicroRNA-29a promotes colorectal cancer metastasis by regulating matrix metalloproteinase 2 and E-cadherin via KLF4[J].Br J Cancer, 2014, 110(2):450-458.doi:10.1038/bjc.2013.724.
[4]Mina L A, Sledge GW Jr.Rethinking the metastatic cascade as a therapeutic target[J].Nat Rev Clin Oncol, 2011, 8(6):325 -332.doi:10.1038/nrclinonc.2011.59.
[5]Coussens L M, Werb Z.Inflammation and cancer[J].Nature, 2002,420(6917):860-867.doi: 10.1038/nature01322.
[6]Fraga MF, Esteller M.Towards the human cancer epigenome: a first draft of histone modifications[J].Cell Cycle, 2005, 4(10):1377-l381.doi: 10.4161/cc.4.10.2113.
[7]Jenuwein T, Allis CD.Translating the histone code[J].Science,2001, 293(5532):1074-1080.doi: 10.1126/science.1063127.
[8]Linggi BE, Brandt SJ, Sun ZW, et al.Translating the histone code into leukemia[J].J Cell Biochem, 2005, 96(5):938-950.doi:10.1002/jcb.20604.
[9]Habu Y, Mathieu O, Tariq M, et al.Epigenetic regulation of transcription in intermediate heterochromatin[J].EMBO Rep, 2006,7(12):1279-1284.doi: 10.1038/sj.embor.7400835.
[10]Magerl C, Ellinger J, Braunschweig T, et al.H3K4 dimethylation in hepatocellular carcinoma is rare compared with other hepatobiliary and gastrointestinal carcinomas and correlates with expression of the methylase Ash2 and the demethylase LSD1 [J].Hum Pathol,2010, 41(2):181-189.doi: 10.1016/j.humpath.2009.08.007.
[11]Gong F, Miller KM.Mammalian DNA repair: HATs and HDACs make their mark through histone acetylation[J].Mutat Res, 2013,750(1/2):23-30.doi: 10.1016/j.mrfmmm.2013.07.002.
[12]Kouzarides T.Chromatin modifications and their function[J].Cell,2007, 128(4):693-705.doi: 10.1016/j.cell.2007.02.005.
[13]Li B, Carey M, Workman JL.The role of chromatin during transcription[J].Cell, 2007, 128(4):707-719.doi: 10.1016/j.cell.2007.01.015.
[14]刘春艳, 孙海晶, 陆军, 等.组蛋白乙酰化与癌症[J].生物化学与生物物理进展, 2003, 30(1):19-23.doi:10.3321/j.issn:1000-3282.2003.01.004.Liu CY, Sun HJ, Lu J, et al.Histone Acetylation and Cancer[J].Progress in Biochemistry and Biophysics, 2003, 30(1):19-23.doi:10.3321/j.issn:1000-3282.2003.01.004.
[15]Balleatar E, Wollfe AP.Methyl-CpG-binding proteins.Targeting specific gene repression[J].Eur J Biochema, 2001, 268(1):1-6.
[16]马旭东, 黄轶群, 肖丽云, 等.急性白血病组蛋白甲基化、乙酰化修饰异常的研究[J].中华血液学杂志, 2010, 31(8):523-526.doi:10.3760/cma.j.issn.0253-2727.2010.08.006.Ma XD, Huang YQ, Xiao LY, et al.Study on aberration in histone methylation and acetylation in acute leukemia[J].Chinese Journal of Hematology, 2010, 31(8):523-526.doi:10.3760/cma.j.issn.0253-2727.2010.08.006.
[17]赵洁, 刘朝晖, 伍玲, 等.人乳腺癌中p21WAF1组蛋白H3、H4乙酰化水平的表达变化[J].肿瘤学杂志, 2014, 20(2):86-90.doi:10.11735/j.issn.1671-170X.2014.02.B002.Zhao J, Liu ZH, Wu L, et al.The Expression Change of Histone H3 and H4 Acetylation on p21WAF1 in Human Breast Cancer[J].Journal of Chinese Oncology, 2014, 20(2):86-90.doi:10.11735/j.issn.1671-170X.2014.02.B002.
[18]Gargalionis AN, Piperi C, Adamopoulos C, et al.Histone modifications as a pathogenic mechanism of colorectal tumorigenesis[J].Int J Biochem Cell Biol, 2012, 44(8):1276-1289.doi: 10.1016/j.biocel.2012.05.002.
[19]Chen C, Zhao M, Yin N, et al.Abnormal histone acetylation and methylation levels in esophageal squamous cell carcinomas[J].Cancer Invest, 2011, 29(8):548-556.doi:10.3109/07357907.2011.597810.
[20]Fraga MF, Ballestar E, Villar-Garea A, et al.Loss of acetylation at Lys16 and trimethylation at Lys20 of histone H4 is a common hallmark of human cancer[J].Nat Genet, 2005, 37(4):391-400.doi:10.1038/ng1531.
[21]Ashktorab H, Belgrave K, Hosseinkhah F, et al .Global histone H4 acetylation and HDAC2 expression in colon adenoma and carcinoma[J].Dig Dis Sci, 2009, 54(10):2109-2117.doi: 10.1007/s10620-008-0601-7.
[22]Tamagawa H, Oshima T, Shiozawa M, et al.The global histone modification pattern correlates with overall survival in metachronous liver metastasis of colorectal cancer[J].Oncol Rep,2012, 27(3):637-642.doi: 10.3892/or.2011.1547.
[23]Roche J, Nasarre P, Gemmill R, et al.Global decrease of histone H3K27 acetylation in ZEB1-induced epithelial to mesenchymal transition in lung cancer cells[J].Cancers (Basel), 2013, 5(2):334-356.doi: 10.3390/cancers5020334.
[24]詹玮, 田甜, 余蕾, 等.蓝莓花青素对HepG2细胞凋亡及组蛋白乙酰化修饰的影响[J].中国普通外科杂志, 2018, 27(1):55-60.doi:10.3978/j.issn.1005-6947.2018.01.009.Zhan W, Tian T, Yu L, et al.Effects of blueberry anthocyanin on apoptosis and histone acetylation in HepG2 cells[J].Chinese Journal of General Surgery, 2018, 27(1):55-60.doi:10.3978/j.issn.1005-6947.2018.01.009.
